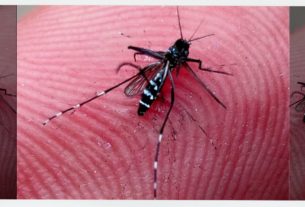
A esclerose múltipla (EM) é uma doença autoimune que afeta o sistema nervoso central e pode causar fadiga, alterações motoras e cognitivas, perda de visão e outros sintomas neurológicos. A condição não tem cura, mas tem tratamento, e o avanço de terapias imunológicas vem permitindo controlar surtos e retardar a progressão da enfermidade.
Um estudo coordenado pela Fiocruz deu um passo importante nessa direção e pode revolucionar a forma como o tratamento é indicado aos pacientes. A pesquisa, publicada na revista Nature Communications, mostrou que é possível prever se uma pessoa com esclerose múltipla responderá bem ao medicamento ‘natalizumabe’ — um dos tratamentos mais comuns contra a doença — antes mesmo do início da terapia.
Para isso, os cientistas do Instituto Oswaldo Cruz (IOC/Fiocruz) desenvolveram um teste simples, feito em laboratório com uma amostra de sangue, que analisa a reação de células de defesa do paciente quando expostas ao medicamento.
Embora ainda não exista um kit clínico pronto para uso em hospitais, o método já funciona integralmente no laboratório. A expectativa é que, nos próximos anos, o procedimento seja simplificado e validado em diferentes populações de pacientes e que possa ser incorporado ao Sistema Único de Saúde (SUS) até 2035.
Além do IOC/Fiocruz, o estudo contou com a participação de cientistas do Instituto de Tecnologia em Imunobiológicos (Bio-Manguinhos/Fiocruz), da Fiocruz Ceará, da Universidade de São Paulo (USP), do Hospital Israelita Albert Einstein e do Instituto de Doenças Infecciosas e Inflamatórias (INFINITy, no acrônimo em inglês), ligado ao Instituto Nacional de Pesquisa em Saúde e Medicina da França (Inserm).
Parte central do trabalho foi realizada durante o doutorado-sanduíche no INFINITy de Beatriz Chaves, aluna do Programa de Pós-graduação em Biologia Computacional e Sistemas do IOC/Fiocruz, e com atividades também na Fiocruz Ceará. “Cerca de 35% dos pacientes não respondem plenamente ao natalizumabe e ainda ficam expostos a riscos e efeitos colaterais. Então começamos a nos perguntar se seria possível entender melhor o efeito do anticorpo nas células e usar isso para prever, antes da terapia, quem realmente vai se beneficiar do medicamento”, contou Beatriz.
Segundo o pesquisador do Laboratório de Pesquisas sobre o Timo do IOC/Fiocruz, Vinicius Cotta, um dos autores do artigo, a descoberta representa um avanço expressivo na luta por melhoria da qualidade de vida dos pacientes com EM. “Poder prever quem vai se beneficiar ou não do tratamento evita a exposição desnecessária a riscos de outros medicamentos, reduz custos e antecipa a troca para terapias mais eficazes, melhorando o prognóstico e a qualidade de vida dos pacientes”, explicou.
Ação do natalizumabe
O artigo O perfil morfológico in vitro de células T prevê a resposta clínica à terapia com natalizumabe em pacientes com esclerose múltipla mostra que as diferenças na reação celular em cada paciente explicam a eficácia do tratamento com o medicamento. Para chegar a essa resposta, entretanto, é preciso entender como atuam três importantes atores: natalizumabe, o subtipo de linfócito T CD8 e as proteínas VLA-4 e VCAM-1 (confira explicações nos próximos parágrafos).
Entre os tratamentos mais comuns contra a esclerose múltipla, o natalizumabe é um imunoterápico usado para impedir que os linfócitos T — células do sistema imunológico — atravessem a barreira que protege o cérebro e a medula espinhal, reduzindo a inflamação que causa os sintomas da doença.
Embora eficaz, o tratamento com o medicamento não funciona igualmente para todas as pessoas. Cerca de 35% dos pacientes continuam apresentando sintomas mesmo após dois anos de uso do natalizumabe. A partir desse cenário, o estudo liderado pelo IOC/Fiocruz desvendou que a chave para antecipar se o paciente responderá bem à terapia está na observação de um tipo específico de linfócito T: as células T CD8.
Essas células são uma espécie de ‘tropa de ataque’ do organismo. Em condições normais, elas atuam no combate a infecções virais e no controle do crescimento de tumores, eliminando células infectadas ou alteradas e desempenhando um papel central na vigilância imunológica.
Entretanto, em doenças autoimunes como a esclerose múltipla, as T CD8 podem confundir componentes do próprio corpo com ameaças e acabar atacando estruturas saudáveis do sistema nervoso, como a mielina — a ‘capa’ que reveste e protege os neurônios.

A pesquisa mostrou que o natalizumabe não age da mesma forma nas células T CD8 de todos os pacientes. Essas diferenças ajudam a explicar por que o medicamento é altamente eficaz para alguns e apresenta efeito limitado em outros casos. A razão está na forma como, em cada paciente, essas células reagem ao bloqueio da proteína VLA-4, que é justamente o alvo do remédio. A VLA-4 é uma molécula que fica na superfície das células T e funciona como um ‘gancho’ que ajuda essas células a grudar nas paredes dos vasos sanguíneos. Já a VCAM-1 é uma proteína de adesão celular, em outras palavras, a ‘argola’ presente nessas paredes, onde o gancho se encaixa.
Quando as duas proteínas se ligam, as células T conseguem se fixar e atravessar a barreira que protege o cérebro e a medula espinhal, o que favorece o processo inflamatório típico da doença. O natalizumabe age interrompendo essa ligação entre a VLA-4 e a VCAM-1, impedindo que as células atravessem a barreira e, assim, reduzindo a inflamação e os demais sintomas da esclerose múltipla.
Se o medicamento não consegue bloquear essa ligação no sistema imunológico do paciente, o tratamento tem efeito limitado. Logo, o objetivo final do estudo foi desenvolver e validar um teste in vitro que preveja a resposta clínica antes do início da terapia, a partir do comportamento de linfócitos T CD8 expostos ao natalizumabe em cada paciente.
Para isso, os pesquisadores coletaram amostras de sangue de pessoas com esclerose múltipla antes do início do tratamento e isolaram as células mononucleares do sangue periférico (PBMCs) — um conjunto que inclui os linfócitos T. Com isso, analisaram, em laboratório, imagens de alta resolução dessas células e usaram algoritmos de aprendizado de máquina para reconhecer padrões de forma, movimentação e organização interna associados à boa ou má resposta ao medicamento.
Com esse teste, abre-se caminho para uma decisão terapêutica mais personalizada, ajudando a escolher a melhor opção para cada paciente e evitando o uso prolongado de tratamentos que não trariam benefício.
Liderança na rede
O artigo foi construído a partir de uma ampla rede de cooperação científica liderada pelo IOC/Fiocruz, que coordenou a integração entre as diferentes frentes do estudo. “O IOC teve um papel central na coordenação científica do projeto em que este estudo se insere. Atuamos como núcleo integrador das distintas áreas, conectando desde o desenho de novos imunoterápicos à utilização de ferramentas de aprendizado de máquina”, contou Cotta.

Além da liderança na rede, o IOC/Fiocruz conduziu testes funcionais de imunologia experimental, além de ter organizado a análise do comportamento das células T CD8 e a interface com a etapa de inteligência artificial para transformar os dados de microscopia em predições de resposta terapêutica.
A Fiocruz Ceará ficou responsável pelo desenho e modelagem de novos anticorpos anti-VLA-4, que bloqueiam a ligação entre as proteínas VLA-4 e VCAM-1; já a equipe de Bio-Manguinhos atuou no desenvolvimento e na produção de novos anticorpos.
No eixo internacional, o Instituto de Doenças Infecciosas e Inflamatórias (INFINITy), da Universidade de Toulouse, conduziu a microscopia de alto conteúdo e o processamento de amostras de pacientes tratados com natalizumabe.
Por fim, a USP e o Hospital Israelita Albert Einstein desenvolveram e aplicaram modelos de aprendizado de máquina para selecionar descritores relevantes das imagens e construir a ferramenta preditiva que antecipa a resposta clínica.
Segundo o pesquisador do Albert Eistein, Helder Nakaya, o uso de inteligência artificial foi fundamental para transformar centenas de informações morfológicas em um modelo viável. “Nós conseguimos reduzir mais de 400 características das células para poucas combinações, que já permitem prever se o paciente vai responder ou não ao tratamento. Sem o aprendizado de máquina, isso ficaria impraticável para virar um teste que pudesse ser validado e aplicado em larga escala”, apontou.
O estudo faz parte de um projeto mais amplo coordenado por Cotta em parceria com o pesquisador de Bio-Manguinhos, Marco Medeiros, voltado ao desenvolvimento de novos imunoterápicos anti-VLA-4 para o tratamento de doenças inflamatórias e autoimunes. “Essa parceria marcou o início do projeto para o desenvolvimento do anticorpo anti-VLA-4. A colaboração entre o IOC, Bio-Manguinhos e a Fiocruz Ceará evidencia a força da integração institucional e mostra como a união de diferentes expertises é fundamental para avançar no desenvolvimento de um insumo biológico inovador para o tratamento da esclerose múltipla”, contou Marco Medeiros.
A iniciativa tem patente depositada em fase de análise internacional e já avança em ensaios pré-clínicos com modelos animais, a partir de um acordo entre a Fiocruz e a Embrapii, com participação da USP Ribeirão Preto. Os próximos passos incluem ampliar a metodologia para novos grupos de pacientes brasileiros, a fim de validar o modelo em diferentes populações, e testar o método em outras doenças inflamatórias e genéticas, nas quais a molécula VLA-4 também desempenha papel central — como a Distrofia Muscular de Duchenne, doença genética ligada ao cromossomo X.
“O cronograma atual prevê que, após os estudos pré-clínicos e clínicos, o produto possa ser registrado e incorporado ao SUS até 2035, consolidando mais um passo da Fiocruz na inovação em saúde e no fortalecimento da produção nacional de biofármacos”, finalizou o pesquisador de Bio-Manguinhos.
(Com informações da Agência Fiocruz) / Foto: Rudson Amorim