Domingo, 19/04/2026 – 14h20
Por Ana Bottallo | Folhapress
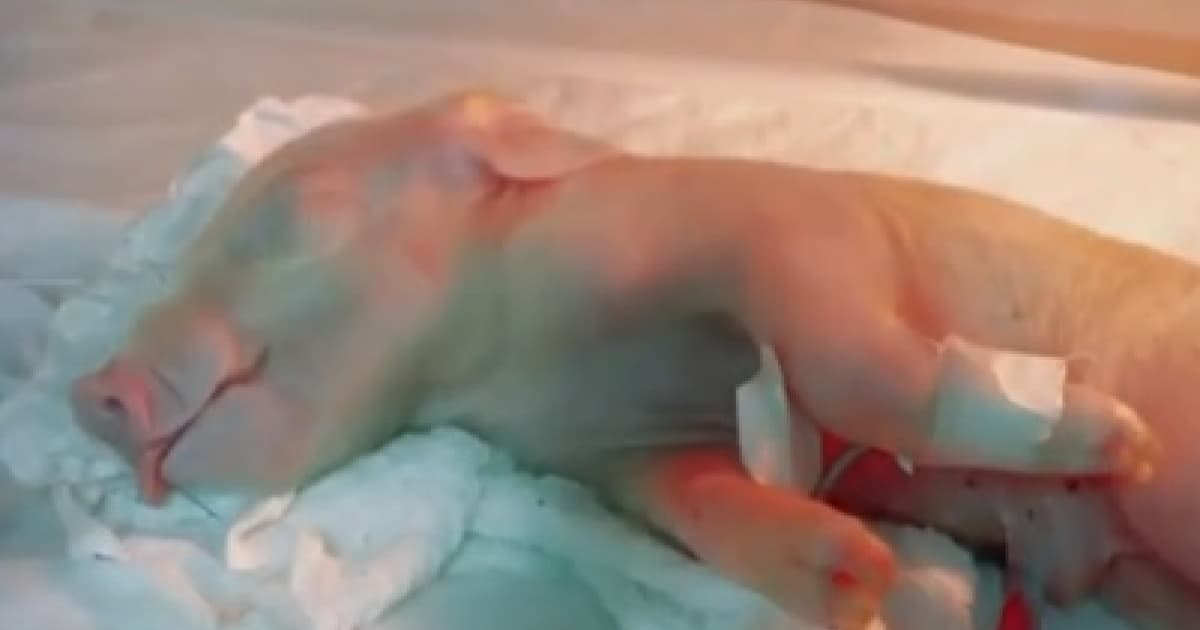
Quase 40 anos após a ovelha Dolly, primeiro mamífero clonado no mundo, uma equipe de cientistas brasileiros celebrou o nascimento de um porco clonado. Ele marca uma etapa importante em um projeto ambicioso: a criação de animais geneticamente modificados para transplante de órgãos em humanos.
O animal nasceu em 24 de março. Está saudável e em uma fazenda em Piracicaba (a 160 km da capital paulista), segundo Ernesto Goulart, pesquisador do Centro de Estudos do Genoma Humano e de Células-Tronco (CEGH-CEL) do Instituto de Biociências da USP.
A equipe responsável pelo feito diz ser o primeiro caso de clonagem da espécie na América Latina.
“São pouquíssimos grupos no mundo que conseguiram a clonagem animal e, entre os animais, o porco é o mais difícil de ser clonado. Como nosso grupo nunca havia trabalhado com esse procedimento, consideramos um sucesso essa etapa”, afirma Goulart.
O leitão não tem as modificações genéticas necessárias para a captação de órgãos, porém é um primeiro passo. A equipe pretende agora implantar embriões geneticamente modificados para xenotransplante no futuro.
“Essa ideia de produzir suínos geneticamente modificados para um transplante em humanos é um sonho bem antigo da medicina, mas ele tinha muitas limitações, porque sempre tem a rejeição hiperaguda”, afirma o pesquisador. A rejeição ocorre porque os humanos carregam anticorpos anti-suínos no sangue. “Em questão de horas, o corpo atacava aquele órgão, e não existiam ferramentas para lidar com isso.”
Com o advento das técnicas de edição gênica, sobretudo a partir de 2012, como o Crispr-Cas 9 (ferramenta para edição molecular descoberta pelas cientistas Emmanuelle Charpentier e Jennifer Doudna, que rendeu às duas o Nobel em Química em 2020), a modificação genética tornou-se mais fácil e também mais acessível a diversos laboratórios.
E representou um novo passo para o transplante de órgãos suínos em humanos.
Até agora, foram realizados quatro xenotransplantes, todos nos Estados Unidos.
O primeiro paciente foi David Bennett, transplantado com um coração suíno em 2022. Ele faleceu 60 dias depois em decorrência de uma rejeição tardia. No ano seguinte, houve o caso de Lawrence Faucette, também paciente cardiológico. Ele morreu seis semanas após o procedimento, mas a causa da morte não foi atribuída ao xenotransplante.
Dois outros pacientes americanos, um homem e uma mulher, receberam rins suínos, sendo que no caso mais recente, ainda sob investigação, o órgão foi retirado alguns dias após a cirurgia, pois o rim do paciente voltou a funcionar.
Outro país que estuda órgãos suínos modificados para xenotransplante é a China. Diante desse cenário, o médico brasileiro Silvano Raia levou uma provocação a seus colegas da USP: ou o Brasil liderava um projeto para criação de animais para xenotransplante, ou se tornaria dependente de órgãos estrangeiros, elevando ainda mais os custos ao SUS (Sistema Único de Saúde).
Foi assim que, sob sua coordenação, nasceu o Centro de Ciência para Desenvolvimento em Xenotransplante, dentro do CEGH-CEL. Integram a equipe o imunologista Jorge Kalil, do InCor (Instituto do Coração da USP), a geneticista Mayana Zatz, do CEGH-CEL, e os pesquisadores Ernesto Goulart, Luiz Caires e Luciano Abreu Brito, também do centro.
“O professor Silvano sabia do meu trabalho com genoma, aqui no centro da USP, e me perguntou: ‘Olha, sei que é uma ideia futurística, mas e se a gente usar suínos como doadores de órgãos?’. E ele indagou se era possível modificar os genes para reduzir a rejeição. Eu respondi que conversaria com a minha equipe”, conta Zatz.
“Nós estamos desenvolvendo uma tecnologia 100% brasileira para levar ao SUS e não depender de órgãos do exterior”, acrescenta a geneticista. Hoje, ela lidera o grupo.
Raia, 96, acompanha as reuniões, mas decidiu deixar a direção geral no fim do ano passado por questões de saúde. O médico é responsável pelo primeiro transplante de fígado no Brasil e pelo primeiro transplante de fígado intervivos no mundo.
‘Ato de coragem’
Os desafios começaram logo após a concepção do projeto. Em um primeiro momento, os cientistas perceberam que inexistia laboratório com os controles sanitários necessários para captação dos órgãos suínos. Era preciso começar a estrutura laboratorial do zero.
O investimento inicial partiu da iniciativa privada (a farmacêutica EMS), mas também da reitoria da USP e da Fapesp (Fundação de Amparo à Pesquisa do Estado de São Paulo). Em menos de três anos, o espaço físico estava construído.
Além dos laboratórios de clonagem e modificação genética, o projeto previa duas unidades para criação dos plantéis suínos: uma no IPT (Instituto de Pesquisas Tecnológicas), com capacidade para até 30 animais, e outra no Instituto de Biociências, para até dez animais.
Em seguida, era preciso dominar as técnicas de clonagem. “Fomos atrás de desenvolver do zero, tivemos esse ato de coragem. Foram diversas tentativas até conseguir fazer nascer o primeiro animal”, diz Goulart.
Para a clonagem, Goulart explica que são utilizadas células de fibroblasto (pele) com uma sequência genética conhecida (doador).
Os óvulos da porca têm seu núcleo removido com o auxílio de um microscópio acoplado de um micromanipulador, uma estrutura com um sensor que faz movimentos muito finos e com uma agulha na ponta menor que um fio de cabelo.
Em seguida, é feita a transferência do fibroblasto para o interior do óvulo. Uma máquina realiza um “choque” na célula, dando início ao processo de embriogênese (formação do embrião), com características idênticas ao do doador. O embrião é, então, implantado na porca para a gestação do filhote clonado.
Outros protocolos já foram mapeados, entre os quais o de modificação genética (são conhecidos hoje três genes suínos que precisam ser desativados para evitar a rejeição pelo receptor humano) e o de controle sanitário (até a ração utilizada para alimentar os porcos deve ser controlada).
Este último, conhecido como SPF (sigla em inglês para livres de patógenos específicos, uma lista de vírus e bactérias potencialmente perigosos que podem contaminar os órgãos), visa garantir que o transplante, quando ocorrer, seja livre de potenciais riscos biológicos.
“Esse foi outro desafio, porque não existia nenhum centro de criação suíno com o nível de controle necessário no hemisfério Sul –a Nova Zelândia tinha um mas fechou. Fomos até a Dinamarca atender essa demanda”, diz Goulart.
Resta, ainda, conseguir a clonagem dos organismos a partir de embriões geneticamente modificados, etapa que os cientistas esperam realizar em breve. Se tudo der certo, os animais clonados vão crescer nas duas unidades do projeto, que também contam com protocolos para captação e transporte dos órgãos.
Demanda
Segundo dados do painel do Sistema Nacional de Transplantes, ligado ao Ministério da Saúde, existem hoje no país 48.773 pessoas na fila aguardando por um transplante de órgão sólido (excluídos pele e córneas). Mais de 90% desses pacientes são para um rim, o órgão que deve ser também o primeiro a ser captado para xenotransplante no projeto.
Embora não arrisque prazos de quando os primeiros órgãos suínos podem ser transplantados em humanos, Goulart diz sentir o peso nos seus ombros. “Queremos atender à demanda, cada um desses pacientes pode ser receptor potencial desses órgãos.”
O maior desafio, agora, é dar continuidade ao projeto e buscar mais recursos. “Os EUA injetam bilhões de dólares na pesquisa com xenotransplante, enquanto nossos recursos aqui são bem mais limitados. Mas o Ministério [da Saúde] e o governo estadual, via Fapesp, entenderam a importância do projeto e estão nos apoiando”, diz Kalil.