Doença genética está associada a infecções recorrentes e potencialmente fatais. Pesquisadores da USP e colaboradores acompanharam 29 transplantados para entender o que acontece com as células de defesa após o tratamento
Karina Ninni, da Agência Fapesp – Domingo, 4 de dezembro de 2022
A anemia falciforme é uma doença genética que causa alterações nos glóbulos vermelhos do sangue (hemácias) e está entre as mais prevalentes no Brasil e no mundo. Um dos tratamentos possíveis é o transplante de células-tronco hematopoiéticas – capazes de se diferenciar em todas as células do sangue – retiradas da medula óssea de um doador saudável. Apesar de o transplante ser atualmente o único tratamento curativo para a doença, pouco se sabe sobre o que acontece com o sistema imune desses pacientes após o procedimento.
Descobertas recentes sobre o tema foram divulgadas por pesquisadores da USP na revista Clinical & Translational Immunology. O artigo tem como foco o sistema imune adaptativo (a imunidade adquirida após o contato com patógenos), particularmente os linfócitos do tipo B (envolvidos na produção de anticorpos) e T (responsáveis pela imunidade celular). Entre os autores estão cientistas do Centro de Terapia Celular (CTC) e da Faculdade de Ciências Farmacêuticas de Ribeirão Preto (FCFRP) da USP, além de colaboradores da França.
Segundo o artigo, após o reset do sistema imunológico promovido pelo transplante, as células B e T se restauraram normalmente. Houve, ainda, um aumento de células B-reguladoras, que podem contribuir para melhorar a regulação imunológica e o equilíbrio da imunidade após o transplante. Também se observou aumento de um subtipo de célula B de memória conhecida como IgM+ (por apresentar a proteína IgM em sua superfície), que é importante para o enfrentamento de infecções.
“Um aspecto muito triste da doença são as diversas complicações clínicas. Uma delas é que os pacientes têm infecções recorrentes, que são a maior causa de morbidade, principalmente entre crianças. Não é raro uma criança diagnosticada com anemia falciforme pegar uma infecção e morrer [sendo o maior problema as infecções bacterianas]. Sabe-se que, além da inflamação crônica acompanhada de episódios de dor, os pacientes têm uma desregulação do sistema imunológico. Mas essa é uma questão ainda muito negligenciada na anemia falciforme”, resume Kelen Cristina Ribeiro Malmegrim, coautora do trabalho. Segundo ela, o sistema imune inato dos pacientes falciformes é bem conhecido, o que não acontece com o sistema imune adaptativo, que inclui as células T e B.
O objetivo da pesquisa foi investigar se o transplante de células-tronco hematopoiéticas poderia melhorar as disfunções imunológicas nos pacientes com anemia falciforme.
“Avaliando os pacientes antes e depois do transplante, vimos que algumas disfunções são corrigidas, mas outras não. Por outro lado, descobrimos que a reconstituição do sistema imune adaptativo após o transplante promove um aumento de células que ajudam a controlar a inflamação crônica, confirmando que o transplante é um recurso terapêutico com resultados excelentes”, explica.
Entendendo a doença

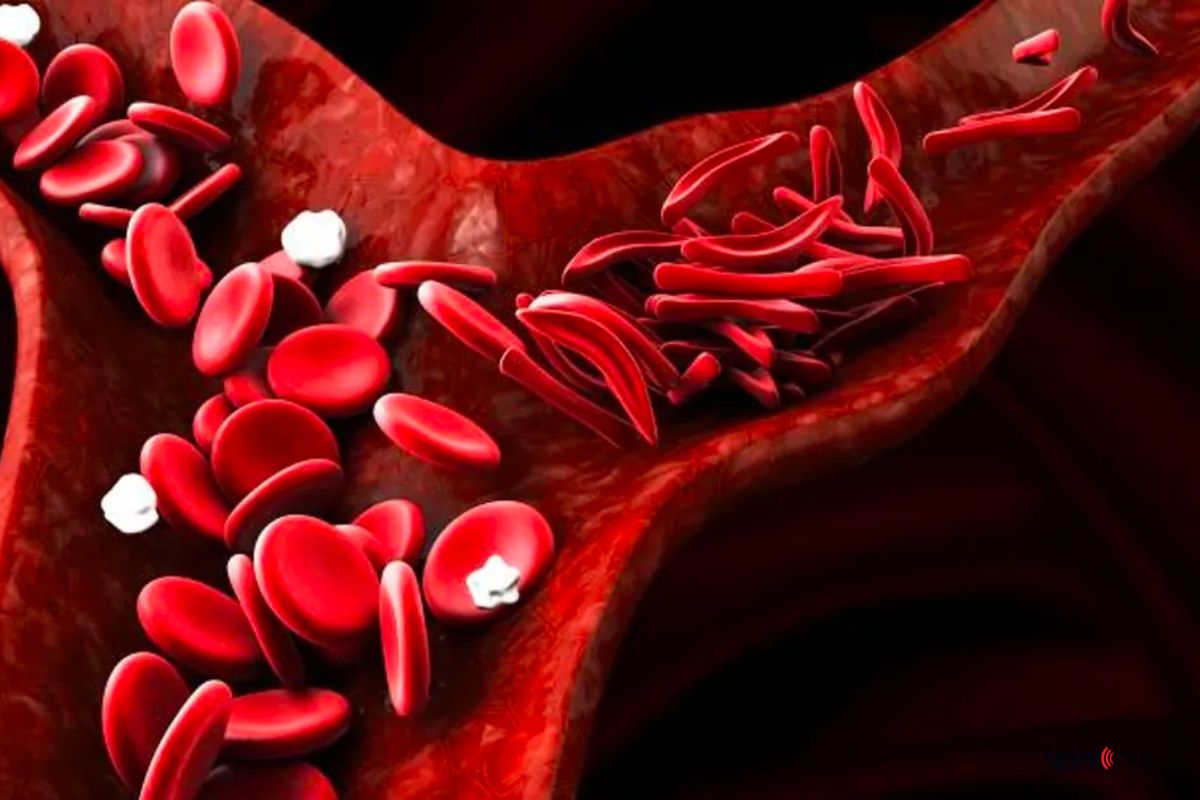
A anemia falciforme é resultado de uma mutação no gene que codifica a hemoglobina – proteína que confere a cor vermelha ao sangue e é responsável pelo transporte de oxigênio. Em portadores da doença, as hemácias assumem a forma de foice depois que o oxigênio é liberado aos tecidos. Em baixas tensões de oxigênio, as células se tornam deformadas, rígidas e propensas a se agregar, ou seja, a formar uma massa celular que adere ao endotélio e dificulta a circulação sanguínea. Nos pacientes falciformes, as hemácias também têm um tempo de vida menor, causando o quadro de anemia.
Os tratamentos convencionais incluem a transfusão sanguínea esporádica (quando os pacientes estão com anemia muito intensa ou em crise) e as transfusões crônicas de hemácias a cada 15 dias em casos muito graves. Outro recurso é um fármaco chamado hidroxiureia, usado também contra outras doenças, como leucemias e outros cânceres. “A hidroxiureia diminui a proliferação celular e aumenta a hemoglobina fetal nas hemácias”, diz.
Quando nascemos, a hemoglobina fetal é predominante nas hemácias e, com o passar dos anos, ela vai dando lugar à hemoglobina tipo A. No caso dos pacientes com anemia falciforme, ela é substituída pela hemoglobina tipo S.
“Ao aumentar a concentração de hemoglobina fetal na hemácia, a hidroxiureia reduz a hemoglobina tipo S. É como uma compensação. Entretanto, os tratamentos convencionais não corrigem as disfunções no sistema imune.”
O estudo foi apoiado pela Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) por meio de bolsas de doutorado no Brasil e no exterior concedidas à farmacêutica Luciana Ribeiro Jarduli-Maciel, primeira autora do artigo. Além das bolsas, o CTC é apoiado no âmbito do programa Centros de Pesquisa, Inovação e Difusão (Cepids).
Disfunções
Segundo Malmegrim, as disfunções no sistema imune dos portadores de anemia falciforme podem ter causas variadas. Algumas podem ser decorrentes da inflamação crônica dos vasos sanguíneos provocada pela doença, que desregula o sistema imune. Porém, outras podem ser causadas por disfunções intrínsecas do sistema imune desses pacientes.
“Uma hemácia contém milhões de moléculas de hemoglobina. Nesses pacientes, quando a hemoglobina libera oxigênio, ela forma polímeros dentro da célula e a hemácia assume a forma de foice. Isso acontece milhares de vezes durante a vida da hemácia e, em algum momento, ela não volta mais à forma original. Essas hemácias em forma de foice entopem os vasos sanguíneos, aglomeram-se e vão se juntando com plaquetas e leucócitos ativados. Elas interagem com outras células, ativam o endotélio, promovendo uma inflamação crônica. E isso pode entupir o vaso e interromper a circulação naquele trecho, provocando isquemia e dor.”
Sabe-se que portadores da anemia falciforme podem ter polimorfismos (variações na sequência do DNA) em outros genes, alguns deles relacionados ao sistema imune, que contribuem para que desenvolvam formas mais graves da doença.
“Uma das disfunções está relacionada à produção excessiva de célula B naive, que são aquelas que não tiveram contato com o antígeno e não carregam a informação sobre o que tem de ser feito [e acabam tomando o espaço das células de memória, que já tiveram contato com o antígeno]. E o transplante melhorou esse aspecto, as células B naive diminuíram e as células B de memória aumentaram. Mas o transplante não corrigiu esse excesso de produção de novas células B naive pela medula óssea dos pacientes. Isso significa que temos de estudar mais detalhadamente esse mecanismo”, explica Malmegrim.
Malmegrim revela que a equipe esperava encontrar alguma disfunção na produção das células T, mas observou que estas são produzidas e exportadas normalmente pelo timo, glândula que fica perto do coração e participa da regulação do sistema imune adaptativo. Somente quando as células T vão para a circulação periférica e encontram moléculas inflamatórias é que sofrem alterações. Entretanto, os pesquisadores suspeitam que alguma alteração acontece no desenvolvimento das células B na medula óssea dos pacientes falciformes.
Estudo clínico
A equipe estudou a reconstituição do sistema imune de 29 pacientes submetidos ao transplante na Unidade de Transplante de Medula Óssea do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto (FMRP) da USP. A idade média do grupo foi 19 anos. Um grupo-controle com 16 pessoas saudáveis também foi acompanhado.
Amostras de sangue periférico foram coletadas dos pacientes antes do transplante e de três em três meses após o procedimento durante dois anos. Os pacientes foram avaliados ainda pelo tamanho do baço (um dos órgãos mais comprometidos pela doença), por análise de prontuários e laudos de ultrassonografia abdominal.
“Todos eles passaram por transplantes alogênicos nos quais a medula do doador era totalmente compatível. E, depois do transplante, estudamos a reconstituição hematopoiética e imunológica”, explica Malmegrim.
Como resume o artigo, o transplante corrige a alteração genética e melhora muito a qualidade de vida dos pacientes, que podem ainda precisar de tratamento para as complicações inflamatórias e imunológicas. Na avaliação de Malmegrim, é muito importante que o procedimento continue sendo feito pelo Sistema Único de Saúde (SUS), onde ocorre desde 2015.
Entretanto, a pesquisadora ressalta que nem todo paciente pode ser transplantado. “Pode não haver doador compatível, por isso transplantes haploidênticos [com células-tronco coletadas do pai, da mãe ou outro membro da família, cuja compatibilidade gira em torno de 50%] já estão sendo realizados mundialmente. Geralmente são pacientes jovens e, quando se trata de uma criança, o transplante é uma decisão difícil para os pais”, explica.
O artigo Allogeneic haematopoietic stem cell transplantation resets T- and B-cell compartments in sickle cell disease patients pode ser acessado em: https://onlinelibrary.wiley.com/doi/10.1002/cti2.1389.
Este texto foi originalmente publicado por Agência Fapesp de acordo com a licença Creative Commons CC-BY-NC-ND. Leia o original aqui.
Fonte: Jornal USP