- Fergus Walsh
- Role,Editor de Medicina, BBC News
A agência regulatória do Reino Unido se tornou a primeira no mundo a aprovar uma terapia genética que promete curar duas doenças que afetam as células sanguíneas.
O novo tratamento contra a doença falciforme e a beta talassemia é pioneira no uso de uma ferramenta de edição genética conhecida como Crispr.
As responsáveis pela técnica — as cientistas Emmanuelle Charpentier e Jennifer Doudna — ganharam o Prêmio Nobel em 2020.
Este avanço é considerado revolucionário para as duas doenças hereditárias que acometem o sangue, ambas desencadeadas por erros no gene da hemoglobina (proteína responsável pelo transporte de oxigênio nas hemácias).
Pessoas com doença falciforme produzem glóbulos vermelhos de formato incomum — parecidos a uma foice.
Isso pode gerar uma série de problemas, uma vez que essas células têm um tempo de vida reduzido e podem bloquear os vasos sanguíneos, o que causa dor e infecções potencialmente fatais.
Já pacientes com beta talassemia não produzem hemoglobina suficiente. Com isso, eles geralmente precisam de transfusões de sangue periódicas, com poucas semanas de intervalo entre as sessões.
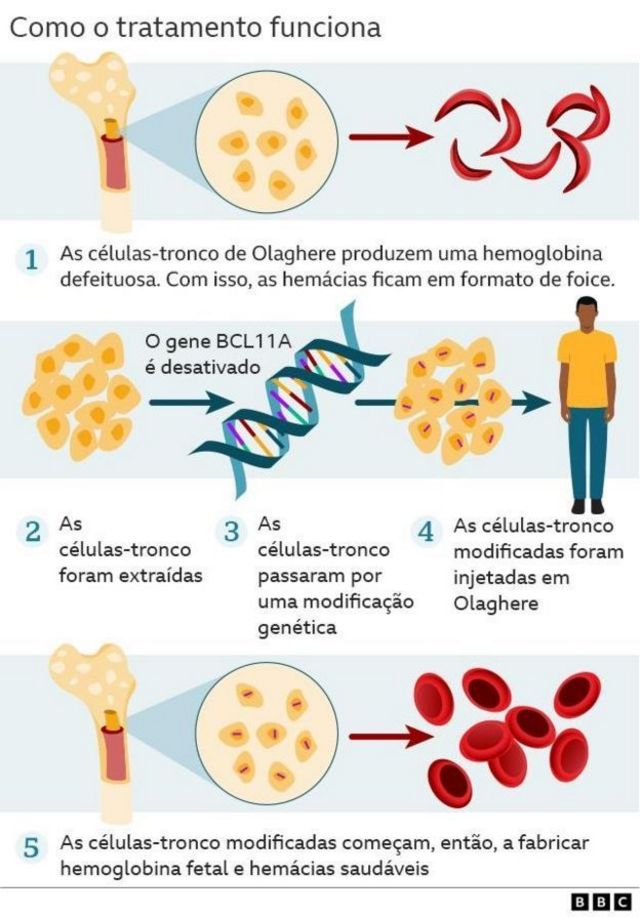
Como a terapia gênica funciona
O DNA é o livro da vida — e os genes trazem as instruções sobre como cada célula do nosso corpo deve funcionar.
A edição de genes permite a manipulação precisa do DNA. O novo tratamento recém-aprovado no Reino Unido envolve a retirada de células-tronco da medula óssea do próprio paciente.
Em laboratório, a ferramenta de edição genética Crispr utiliza espécies de tesouras moleculares para fazer cortes precisos no DNA dessas células. Isso permite desativar os genes defeituosos que estão por trás dos problemas de saúde.
As células modificadas são, então, infundidas de volta no organismo. Com isso, o corpo começa a produzir hemoglobina dentro dos padrões esperados.
Nos ensaios clínicos que serviram de base para a aprovação, 28 dos 29 pacientes com anemia falciforme deixaram de apresentar dores intensas e 39 dos 42 pacientes com beta talassemia não precisam mais das transfusões de sangue há pelo menos um ano. Espera-se que a terapia gênica possa ser uma solução permanente para eles.
Os testes com a nova terapia continuam a acontecer no Reino Unido, nos EUA, na França, na Alemanha e na Itália.
Cerca de 15 mil pessoas no Reino Unido têm doença falciforme, a maioria com antecedentes familiares africanos ou caribenhos. Quase 300 bebês nascem no Reino Unido com doença falciforme todos os anos.
No Brasil, onde ainda não há previsão para a chegada da nova terapia, o Ministério da Saúde estima entre 60 a 100 mil indivíduos com anemia falciforme. Cerca de 3 mil novos casos são diagnosticados todos os anos.
“Dados do Sistema de Informações de Mortalidade do SUS apontam que, entre 2014 e 2019, a maior parte dos pacientes com doença falciforme no Brasil faleceu na segunda década de vida (20 aos 29 anos). O Brasil registra mais de um óbito de por dia em decorrência da doença e mantém uma média de um óbito por semana em crianças de 0 a 5 anos”, aponta o ministério.
Mais de mil pessoas no Reino Unido são afetadas pela beta talassemia. Elas geralmente têm origens familiares relacionadas a regiões como o Mediterrâneo, o Sudeste Asiático e o Oriente Médio.
O Ministério da Saúde calcula que cerca de mil brasileiros apresentam as formas mais graves de talassemia.
“Tanto a doença falciforme quanto a beta talassemia são condições dolorosas que duram a vida toda e, em alguns casos, podem ser fatais”, pontua Julian Beach, diretor executivo interino de Qualidade e Acesso aos Cuidados de Saúde da Agência Reguladora de Medicamentos e Produtos de Saúde (MHRA) do Reino Unido.
“Até o momento, um transplante de medula óssea — que deve vir de um doador estreitamente compatível e apresenta um risco de rejeição — era a única opção de tratamento permanente.”
A partir de agora, segundo Beach, o arsenal terapêutico contra as duas enfermidades se ampliou com a aprovação da primeira terapia genética, cujo nome comercial é Casgevy.
Nos ensaios clínicos, foi “descoberto que ela restaura a produção saudável de hemoglobina na maioria dos participantes com doença falciforme e beta talassemia que dependem de transfusões, o que alivia os sintomas”, disse ele.

‘Sinto que renasci’
Jimi Olaghere pensou que precisaria esperar décadas para se livrar da doença falciforme.
Ele deu um depoimento à BBC News em 2022, depois de se tornar um dos primeiros sete pacientes a se beneficiar do novo tratamento de edição genética nos Estados Unidos.
“É como nascer de novo”, declarou Olaghere no ano passado.
Ele disse sobre como sentiu que o tratamento havia mudado sua vida. “Quando olho para trás, penso: ‘Não acredito que vivi com isso’.”
Olaghere vivia com anemia falciforme desde a infância. “Você sempre tem que estar com uma mentalidade de guerra, sabendo que seus dias serão repletos de desafios.”
“A doença falciforme é uma condição incrivelmente debilitante, causa dor significativa às pessoas e leva à mortalidade precoce”, destacou John James, presidente da Sickle Cell Society, uma associação que realiza ações sobre a anemia falciforme no Reino Unido.
“Atualmente, existem poucos medicamentos disponíveis para os pacientes. Por isso, saúdo a notícia de que um novo tratamento foi considerado seguro e eficaz, com o potencial de melhorar significativamente a qualidade de vida de tantas pessoas.”
O preço do Casgevy ainda não foi definido, mas especula-se que a terapia possa custar 1 milhão de libras (R$ 6 milhões) ou mais — o que pode ser considerado um preço muito alto para os serviços públicos de saúde.
Em abril, o Instituto de Revisão Clínica e Econômica dos Estados Unidos calculou que o tratamento só seria rentável caso seu preço ultrapassasse a casa de 1,5 milhão de libras (R$ 9 milhões).
O Casgevy é um tratamento personalizado e único, feito a partir de ajustes nas células do próprio paciente — o que torna o processo caro e demorado. Além disso, os responsáveis também acrescentam na conta os custos com a pesquisa e o desenvolvimento.
A Vertex, empresa farmacêutica americana responsável pela terapia gênica, deseja que o produto seja utilizado de forma ampla. Para isso, precisará estabelecer um preço que os serviços públicos de saúde estejam preparados para pagar.
Fonte: BBC Brasil